Преглед садржаја
Хемија за децу
Раствори и растварање
Шта је раствор?Раствор је специфична врста смеше у којој се једна супстанца раствара у другу. Раствор је исти, или уједначен, што га чини хомогеном смешом. Идите овде да бисте сазнали више о смешама.
Раствор има одређене карактеристике:
- Уједначен је или хомоген у целој смеши
- Постојан је и не мења се током времена или се таложе
- Честице растворене супстанце су толико мале да се не могу одвојити филтрирањем
- Молекули растворене супстанце и растварача се не могу разликовати голим оком
- Не распршују се сноп светлости
Један пример раствора је слана вода која је мешавина воде и соли. Не можете видети со, а со и вода ће остати раствор ако се оставе саме.
Делови раствора
- Растворена - растворена супстанца је супстанца која се растворен другом супстанцом. У примеру изнад, со је растворена супстанца.
- Растварач – Растварач је супстанца која раствара другу супстанцу. У горњем примеру, вода је растварач.
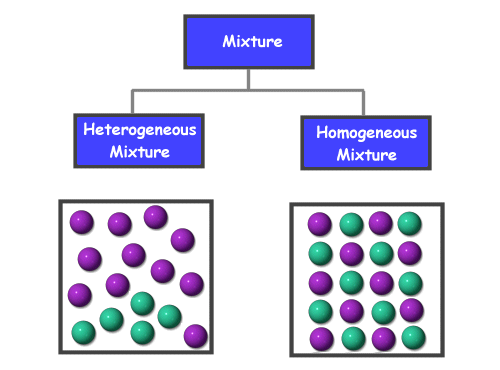
Раствор је врста хомогене смеше
Растварање
Раствор се прави када се једна супстанца која се зове раствор "раствори" у другу супстанцу која се зове растварач. Растварање је када се растворена супстанца распада одвећи кристал молекула у много мање групе или појединачне молекуле. Овај распад је узрокован доласком у контакт са растварачем.
У случају слане воде, молекули воде одвајају молекуле соли из веће кристалне решетке. Они то раде тако што повлаче јоне, а затим окружују молекуле соли. Сваки молекул соли и даље постоји. Управо је сада окружена молекулима воде уместо да је фиксирана за кристал соли.
Растворљивост
Растворљивост је мера колико растворене супстанце може да се раствори у литру растварача. Размислите о примеру воде и соли. Ако наставите да сипате со у воду, у неком тренутку вода неће моћи да раствори со.
Засићено
Када раствор достигне тачку где више не може да раствори раствор сматра се "засићеним". Ако засићени раствор изгуби нешто растварача, тада ће почети да се формирају чврсти кристали растворене супстанце. Ово се дешава када вода испари и кристали соли почну да се формирају.
Концентрација
Концентрација раствора је пропорција растворене супстанце и растварача. Ако у раствору има много растворене супстанце, онда је он „концентрисан“. Ако постоји мала количина растворене супстанце, онда се за раствор каже да је „разблажен“.
Меша се и не може да се меша
Када се две течности могу помешати да би се формирао решење називају се "мешљивим". Ако две течностине могу се мешати да би се формирао раствор називају се "немешљивим". Пример течности које се мешају су алкохол и вода. Пример течности које се не мешају су уље и вода. Да ли сте икада чули за изреку „уље и вода се не мешају“? То је зато што се не мешају.
Занимљиве чињенице о решењима
- Постоји растварач који се зове краљевска вода који може да раствори племените метале укључујући злато и платину.
- Не можете видети сноп светлости када га сијате кроз право решење. То значи да магла није решење. То је колоид.
- Раствори могу бити течни, чврсти или гасовити. Пример чврстог раствора је челик.
- Чврсте материје су генерално растворљивије на вишим температурама.
- Газирана пића се праве растварањем гаса угљен-диоксида у течност под високим притиском.
Решите квиз са десет питања на овој страници.
Послушајте читање ове странице:
Ваш претраживач не подржава аудио елемент.
Још предмета хемије
| Материја |
Атом
Молекули
Изотопи
Чврсте материје, течности, гасови
Топљење и кључање
Хемијско везивање
Хемијске реакције
Такође видети: Биографија за децу: Кублај КанРадиоактивност и зрачење
Именовање једињења
Смеше
Смеше за одвајање
Раствори
Киселине и базе
Кристали
Метали
Соли иСапуни
Вода
Такође видети: Древни Рим за децу: Колосеум
Речник и термини
Опрема за лабораторије за хемију
Органска хемија
Чувени хемичари
Елементи и периодни систем
Елементи
периодични систем
наука &гт;&гт; Хемија за децу


