Sadržaj
Hemija za djecu
Otopine i otapanje
Šta je otopina?Otvor je specifična vrsta mješavine u kojoj je jedna supstanca otopljena u drugu. Rastvor je isti, ili ujednačen, što ga čini homogenom smjesom. Idite ovdje da saznate više o mješavinama.
Otopina ima određene karakteristike:
- Ujednačena je ili homogena u cijeloj smjesi
- Postojana je i ne mijenja se tokom vremena ili se talože
- Čestice otopljene tvari su toliko male da se ne mogu odvojiti filtriranjem
- Molekule otopljene tvari i rastvarača ne mogu se razlikovati golim okom
- Ne raspršuju se snop svjetlosti
Jedan primjer rješenja je slana voda koja je mješavina vode i soli. Ne možete vidjeti sol, a sol i voda će ostati otopina ako se ostave same.
Dijelovi otopine
- Otopljena otopina - Otopljena tvar je supstanca koja se rastvoren drugom supstancom. U gornjem primjeru, sol je otopljena supstanca.
- Otapalo - Rastvarač je supstanca koja otapa drugu supstancu. U gornjem primjeru, voda je rastvarač.
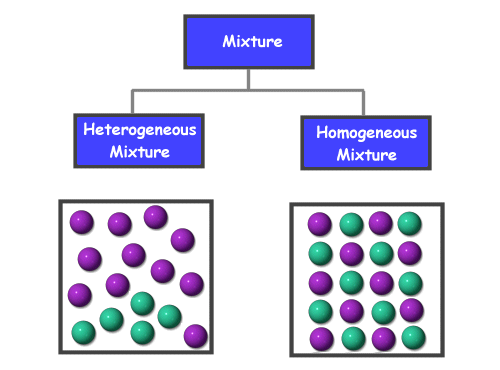
Otvor je vrsta homogene smjese
Otapanje
Otvor se pravi kada se jedna supstanca koja se zove otopljena tvar "rastvori" u drugu supstancu koja se zove rastvarač. Otapanje je kada se rastvorena supstanca raspadne izveći kristal molekula u mnogo manje grupe ili pojedinačne molekule. Ovaj raspad je uzrokovan dolaskom u kontakt sa rastvaračem.
U slučaju slane vode, molekuli vode odvajaju molekule soli iz veće kristalne rešetke. Oni to rade tako što povlače jone, a zatim okružuju molekule soli. Svaki molekul soli i dalje postoji. Upravo je sada okružena molekulima vode umjesto da je fiksirana na kristal soli.
Rastvorljivost
Rastvorljivost je mjera koliko se otopljene tvari može otopiti u litri rastvarača. Razmislite o primjeru vode i soli. Ako nastavite sipati sol u vodu, u nekom trenutku voda neće moći otopiti sol.
Zasićeno
Kada otopina dostigne tačku tamo gde ne može da rastvori više otopljene supstance smatra se "zasićenim". Ako zasićena otopina izgubi nešto otapala, tada će se početi formirati čvrsti kristali otopljene tvari. Ovo se događa kada voda ispari i kristali soli počnu da se formiraju.
Koncentracija
Koncentracija otopine je udio otopljene tvari i otapala. Ako u otopini ima puno otopljene tvari, onda je ona "koncentrirana". Ako postoji mala količina otopljene tvari, tada se za otopinu kaže da je "razrijeđena."
Mješa se i ne može se miješati
Kada se dvije tekućine mogu pomiješati da formiraju rješenje se nazivaju "mješljivim". Ako dvije tečnostine mogu se mešati da bi se formirao rastvor, nazivaju se "nemešljivim". Primjer tekućina koje se miješaju su alkohol i voda. Primjer tekućina koje se ne miješaju su ulje i voda. Jeste li ikada čuli za izreku "ulje i voda se ne miješaju"? To je zato što se ne miješaju.
Zanimljive činjenice o rješenjima
- Postoji rastvarač zvan kraljevska akva koja može otopiti plemenite metale uključujući zlato i platinu.
- Ne možete vidjeti snop svjetlosti kada ga obasjavate kroz pravo rješenje. To znači da magla nije rješenje. To je koloid.
- Otvori mogu biti tekući, čvrsti ili plinoviti. Primjer čvrste otopine je čelik.
- Čvrste tvari su općenito topljivije na višim temperaturama.
- Gazirana pića se proizvode otapanjem plina ugljičnog dioksida u tekućinu pod visokim pritiskom.
Rešite kviz s deset pitanja na ovoj stranici.
Poslušajte čitanje ove stranice:
Vaš preglednik ne podržava audio element.
Više predmeta hemije
| Materije |
Atom
Molekule
Izotopi
Čvrste tvari, tekućine, plinovi
Topljenje i ključanje
Vidi_takođe: Mjesec decembar: rođendani, historijski događaji i prazniciKemijsko vezivanje
Kemijske reakcije
Vidi_takođe: Velika depresija: Hoovervilles za djecuRadioaktivnost i zračenje
Imenovanje spojeva
Smjese
Smjese za odvajanje
Otopine
Kiseline i baze
Kristali
Metali
Soli iSapuni
Voda
Pojmovnik i pojmovi
Oprema za laboratorije za hemiju
Organska hemija
Poznati hemičari
Elementi i periodni sistem
Elementi
periodični sistem
nauka >> Hemija za djecu


