目次
子供のための化学
溶液と溶解
解決策とは?溶液は、ある物質が別の物質に溶解している特定のタイプの混合物です。 溶液は、全体が同じ、または均一であるため、均質な混合物となります。 混合物についてもっと知りたい方はこちらへどうぞ。
ソリューションには、ある特徴があります。
- 混合物全体が均一である(ホモジニアスである)。
- 経年変化や沈降がなく、安定していること
- 溶質粒子が非常に小さく、フィルターで分離できない場合
- 溶質と溶媒の分子は肉眼では区別できない
- 光線を散乱させない
水と塩の混合物である塩水は、水溶液の一例です。 塩が見えないので、塩と水は放っておいても水溶液であり続けます。
ソリューションのパーツ
- 溶質とは、他の物質によって溶かされる物質のことで、上記の例では塩が溶質となる。
- 溶媒 - 溶媒は、他の物質を溶解する物質である。 上記の例では、水が溶媒である。
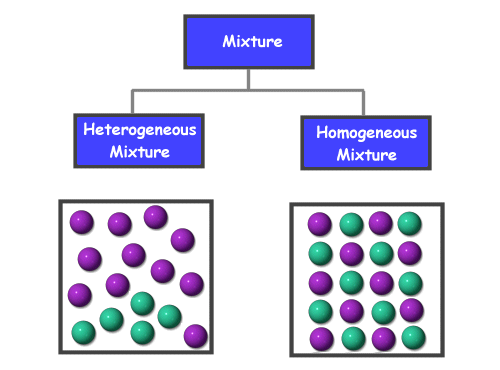
溶液は均一な混合物の一種である
ディゾルブ
溶液は、溶質と呼ばれる物質が溶媒と呼ばれる物質に「溶ける」ことによって作られます。 溶けるとは、溶質が分子の大きな結晶から、より小さなグループまたは個々の分子に分解されることです。 この分解は、溶媒と接触することによって引き起こされます。
塩水では、水分子が塩の分子を結晶格子から引き離し、イオンを引き離して塩の分子を取り囲む。 塩の分子は、塩の結晶に固定されているのではなく、水分子に取り囲まれているだけで、依然として存在しているのだ。
溶解性
溶解度とは、1リットルの溶媒にどれだけの溶質を溶かすことができるかを示す指標です。 水と塩の例で考えると、水に塩を入れ続けると、いつかは水が塩を溶かすことができなくなります。
飽和状態
飽和溶液から溶媒が失われると、溶質の固体結晶が生成されます。 水が蒸発して塩の結晶が生成されるのはこの現象です。
コンセントレーション
溶液の濃度は、溶質と溶媒の割合です。 溶液中の溶質が多ければ "濃縮"、溶質が少なければ "希釈 "と言われます。
混和性・非混和性
混ぜることができる液体を「混和性」、混ぜることができない液体を「不混和性」といいます。 混和性のある液体の例として、アルコールと水、混和性のない液体の例として油と水があります。 油と水は混ざらない」という言葉を聞いたことがありませんか? これは混和性がないためです。
ソリューションに関する興味深い事実
- 金やプラチナなどの貴金属を溶かすことができるアクアレギアという溶剤があります。
- つまり、霧は溶液ではなく、コロイドなのです。
- 溶液には液体、固体、気体があり、固体の例として鉄があります。
- 固形物は一般に温度が高いほど溶けやすくなります。
- 炭酸飲料は、炭酸ガスを高圧で液体に溶かし込んだものです。
このページで10問のクイズに挑戦してください。
関連項目: アメリカ史:世界恐慌このページの朗読をお聞きください。
お使いのブラウザは、オーディオ要素に対応していません。
その他の化学系科目
| 事項 |
アトム
分子
同位体
固体、液体、気体
溶融と沸騰
化学結合
化学反応
放射能・放射性物質
化合物の命名
ミクスチャー
混合物の分離
ソリューション
酸・塩基
水晶
金属
塩と石鹸
水
用語集・用語解説
化学実験装置
有機化学
有名な化学者
元素と周期表
エレメント
周期表
サイエンス>> ケミストリー・フォー・キッズ


