Содржина
Хемија за деца
Решенија и растворање
Што е раствор?Растворот е специфичен тип на смеса каде што една супстанција се раствора во друга. Растворот е ист или униформен, низ кој прави хомогена смеса. Одете овде за да дознаете повеќе за мешавините.
Решението има одредени карактеристики:
- Тоа е еднолично или хомогено, низ целата смеса
- Тој е стабилен и не се менува со текот на времето или се таложат
- Честичките на растворената супстанција се толку мали што не можат да се одвојат со филтрирање
- Молекулите на растворената супстанција и растворувачот не можат да се разликуваат со голо око
- Не се расфрлаат зрак светлина
Еден пример за раствор е солената вода која е мешавина од вода и сол. Не можете да ја видите солта, а солта и водата ќе останат раствор ако се остават сами.
Делови од растворот
- Растворени материи - растворената супстанца е супстанцијата што се растворени со друга супстанција. Во горниот пример, солта е растворената супстанција.
- Растворувач - Растворувачот е супстанцијата што ја раствора другата супстанција. Во примерот погоре, водата е растворувач.
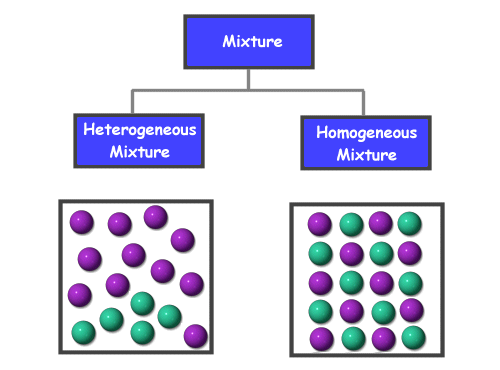
Растворот е вид на хомогена смеса
Распуштање
Растворот се добива кога една супстанција наречена растворена супстанција „се раствора“ во друга супстанција наречена растворувач. Распуштање е кога растворената супстанција се распаѓа одпоголем кристал на молекули во многу помали групи или поединечни молекули. Ова распаѓање е предизвикано од доаѓањето во контакт со растворувачот.
Во случај на солена вода, молекулите на водата ги отцепуваат молекулите на сол од поголемата кристална решетка. Тие го прават тоа со повлекување на јоните и потоа со опкружување на молекулите на солта. Секоја молекула на сол сè уште постои. Само сега е опкружен со молекули на вода наместо да се фиксира на кристал од сол.
Растворливост
Растворливоста е мерка за тоа колку растворена супстанца може да се раствори во литар на растворувач. Размислете за примерот на вода и сол. Ако продолжите да истурате сол во вода, во одреден момент водата нема да може да ја раствори солта.
Заситена
Исто така види: Биографија: Ана Франк за децаКога растворот ќе достигне точка каде што не може да раствори повеќе растворена супстанција се смета за „заситен“. Ако заситениот раствор изгуби малку растворувач, тогаш ќе почнат да се формираат цврсти кристали на растворената супстанција. Тоа е она што се случува кога водата испарува и кристалите на солта почнуваат да се формираат.
Концентрација
Концентрацијата на растворот е соодносот на растворената супстанција со растворувачот. Ако во растворот има многу растворена супстанција, тогаш таа е „концентрирана“. Ако има мала количина на растворена супстанција, тогаш се вели дека растворот е „разреден“. решение тие се нарекуваат "мешање". Ако две течностине може да се мешаат за да се формира раствор тие се нарекуваат „немешачки“. Пример за мешани течности се алкохолот и водата. Пример за течности што не се мешаат се маслото и водата. Дали некогаш сте ја слушнале изреката „маслото и водата не се мешаат“? Тоа е затоа што тие не се мешаат.
Интересни факти за решенијата
- Постои растворувач наречен aqua regia кој може да ги раствори благородните метали вклучувајќи злато и платина.
- Не можете да видите зрак светлина кога ќе го заблескате низ вистинско решение. Ова значи дека маглата не е решение. Тоа е колоид.
- Решенијата можат да бидат течни, цврсти или гасови. Пример за цврст раствор е челикот.
- Цврсти материи генерално се порастворливи на повисоки температури.
- Газираните пијалоци се добиваат со растворање на гасот на јаглерод диоксид во течност при висок притисок.
Поставете квиз со десет прашања на оваа страница.
Слушајте читање на оваа страница:
Вашиот прелистувач не поддржува аудио елемент.
Повеќе предмети по хемија
| Материја |
Атом
Молекули
Изотопи
Цврсти материи, течности, гасови
Топење и вриење
Хемиско поврзување
Хемиски реакции
Радиактивност и зрачење
Именување соединенија
Мешавини
Исто така види: Празници за деца: Ден на независноста (четврти јули)Одвојувачки мешавини
Решенија
Кселини и бази
Кристали
Метали
Соли иСапуни
Вода
Речник и термини
Опрема за хемиска лабораторија
Органска хемија
Познати хемичари
Елементи и периодична табела
Елементи
Периодичен систем
Наука >> Хемија за деца


